![]()

Dr Richard Hunt
CAPÍTULO DIECINUEVE - HEPATITISPARTE DOS – ENFERMEDAD DE TRANSMISIÓN PARENTERAL
HEPATITIS B, C, D y G
VIDEOCONFERENCIA
EN INGLÉS
 Figura 1
Figura 1Virus de la Hepatitis B CDC
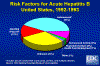 Figura 2
Figura 2
Factores de Riesgo para Hepatitis B Aguda, Estados Unidos, 1992-1993 CDC
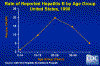 Figura 3
Figura 3
Tasa de Casos de Hepatitis B reportados de acuerdo al grupo etáreo, Estados
Unidos, 1990. CDC
HEPATITIS SÉRICA - HEPATITIS B
El virus de la Hepatitis B (VHB) (figura 1) pertenece a la familia de los
hepadnavirus y tienen un genoma de ADN que se replica vía un intermediario
de ARN. Dependiendo de la respuesta inmune del paciente, la infección por el
VHB puede ser asintomática, crónica o aguda. Al igual que con el VHA, los
humanos son el único reservorio para el VHB. El virus se disemina por el
contacto con fluidos corporales (usualmente contaminación sanguínea, aunque
también se contagia por el semen u otras secreciones tales como fluidos
vaginales, sangre menstrual, saliva y leche materna). Aunque la inyección de
sangre (como resultado de adicción a drogas intravenosas o por el uso de
otros instrumentos contaminados con sangre tales como las navajas) es la vía
más común de infección, el virus también se puede contraer por contacto
sexual (particularmente el de hombre a hombre) y perinatalmente (figura 2).
Según el Centro de Control y Prevención de Enfermedades (CDC, en inglés)
aproximadamente 78,000 personas en los Estados Unidos fueron infectadas con
el VHB en el 2,001 y casi 5,000 personas mueren cada año de alguna
enfermedad asociada al VHB, Una de cada 20 personas en los Estados Unidos se
infecta con el VHB alguna vez en sus vidas y la tasa más alta de infección
la tienen los adultos jóvenes (figura 3 y 4). Cerca del 5% de las personas
infectadas con el VHB manifiestan una infección crónica y hay más de un
millón de norteamericanos con hepatitis B crónica. Casi un cuarto de estos
pacientes crónicamente enfermos morirá por alguna forma de enfermedad
hepática. Como resultado la excelente vacuna actualmente disponible, el
número de infecciones agudas por hepatitis B en ha disminuido en los Estados
Unidos (figura 5).
 Figura 4
Figura 4Edad de adquisición de Infección aguda y crónica de VHB, Estados Unidos, Estimados de 1989 CDC
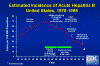 Figura 5
Figura 5
Incidencia estimada de Hepatitis B Aguda, Estados Unidos, 1978-1995 CDC
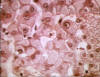 Figura 6
Figura 6
Portados de antígeno australiano, hepatocito con apariencia de vidrio
esmerilado © Archivo de Imágenes Biomédicas de Bristol. Usado con
autorización
Patología
El VHB entra al cuerpo por el torrente sanguíneo y se dirige a los hepatocitos, presuntamente porque su receptor se encuentra predominantemente en estas células. Hay muy poco efecto citopático y la proporción de aparición de los síntomas depende de la dosis inicial del virus. El periodo de incubación es de 60-90 días (con un rango de 45-180 días), aunque la replicación viral inicia unos cuantos días después de la infección. El primer signo de infección es la aparición característica de los antígenos HBs (HBsAg) en las células infectadas (apariencia de vidrio esmerilado (figura 6)). Al igual como sucede con otros virus de hepatitis, los síntomas son mediados por la respuesta inmune, resultando de la inflamación de la respuesta mediada por células (células T citotóxicas) al HBsAg en la superficie de los hepatocitos. Esto también resuelve la enfermedad. Los síntomas incluyen ictericia (figura 7), fatiga, dolor abdominal, pérdida de apetito, náusea, vómitos y dolor articular. Si la respuesta mediada por células es débil, los síntomas son leves pero la infección no se resuelve y sobreviene una hepatitis crónica. Este es el caso frecuente de los pacientes más jóvenes que tienen una menor inmunidad mediada por células. Casi el 10% de los pacientes menores de 5 años de edad manifiestan una enfermedad clínica (ejemplificada por la ictericia) aunque el 30-90% de los pacientes jóvenes infectados mantienen una infección crónica. En los picantes mayores de 5 años de edad, el 30-50% tienen una enfermedad clínica y casi un tercio son asintomáticos. En estos pacientes, 2 a 10% pasan a tener una infección crónica (figura 8).
La infección crónica del VHB puede llevar a hepatitis crónica. Esto conlleva cirrosis hepática en una cuarta parte de los pacientes en un tiempo de 5 años. De estos pacientes, casi un cuarto desarrollará carcinoma hepatocelular (figura 9) o fallo hepático. Ambas de estas son fatales en la ausencia de un transplante hepática.
 Figura 7
Figura 7Hepatitis Viral Aguda CDC
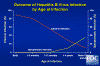 Figura 8
Resultado de Infección por el Virus de la Hepatitis B según la edad de
infección CDC
Figura 8
Resultado de Infección por el Virus de la Hepatitis B según la edad de
infección CDC
 Figura 9 Mujer de Jemer (Camboya) quien murió por un hepatoma,
cuatro meses después de llegar a un campo de refugiados en Tailandia CDC
Figura 9 Mujer de Jemer (Camboya) quien murió por un hepatoma,
cuatro meses después de llegar a un campo de refugiados en Tailandia CDC
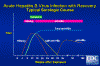 Figura 10
Figura 10Infección aguda del virus de hepatitis B con recuperación – curso serológico típico CDC
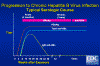 Figura 11
Figura 11
Progresión a Infección crónica de hepatitis B – Curso serológico típico CDC
Inmunología
Una respuesta inmune mediada por células a una infección por VHB resulta en la reacción de las células T citotóxicas contra los antígenos tanto de superficie (HBsAg) como internos (HBcAg y HBeAg). La respuesta humoral también es protectora. Además de viriones intactos, las células infectadas por VHB descaman partículas que se componen principalmente de agregados de antígeno HbS. Esto se combina con un bloque de anticuerpos anti-HbS, limitando así la respuesta humoral. La gran cantidad de complejos anticuerpo – HbsAg causa reacciones de hipersensibilidad tipo III y resulta en eritema, artralgia y daño renal. No obstante, los anticuerpos confieren de inmunidad de por vida y la presencia de HBeAg es indicativa de baja transmisibilidad.
En las infecciones agudas por VHB, los síntomas permanecen por 10 a 20 semanas luego de la infección. Antes de la aparición de los síntomas los antígenos HBsAg y HBeAg son detectables en el torrente sanguíneo. Los anticuerpos contra el HBeAg son detectables cerca de 4 meses luego de la infección. Inicialmente, los anticuerpos anti-HBcAg son IgM pero esto decrece aunque el total de anti-HBcAg continua a niveles altos. El HBsAg es detectable en sangre de uno a seis meses después de la infección, pero el anti-HBsAg sólo es detectable desde los 8 meses. Por tanto, hay una "ventana" durante la cual ni HBsAg ni anti-HBsAg pueden ser detectados. Como consecuencia de la respuesta inmune, la enfermedad se resuelve en la mayoría de los pacientes (figura 10).
En una infección crónica, HBsAg y HBeAg son detectables a través del curso de la infección. Los anti-HBcAg (que inicialmente son IgM) y los anti-HBeAg también se pueden detectar (figura 11).
Carcinogénesis
El VHB es la mayor causa de carcinoma hepatocelular a nivel mundial (figura 9); de hecho, la infección con VHB puede ser la causa de más del 80% de los casos de carcinomas hepatocelulares primarios a nivel mundial. Este es el caso particular cuando los pacientes son HBeAg-positivos. En Taiwán en donde el 15% de la población es portadora, los portadores de HBsAg tienen un riesgo de carcinoma hepatocelular casi 217 veces el de un no-portador. Casi la mitad de las muertes de portadores de HBsAg son causadas por cirrosis hepática o carcinoma hepatocelular en comparación con el 2% de la población general. Para más información sobre los hepadnavirus y el cáncer, refiérase a los capítulos seis y dieciocho.
 Figura 12
Figura 12Distribución geográfica de la infección crónica del VHB CDC
Epidemiología
El VHB se encuentra globalmente (figura 12). La mayor incidencia de seropositividad para el VHB (anti-HBsAg) está en el África sub-Sahariana, el Extremo Oriente (China, Malasia, Indonesia, Filipinas, Papúa Nueva Guinea etc.). Otros niveles altos (más de un 8% de la población infectado) se ve en el norte de América de Sur, el norte de Canadá y Alaska y Groenlandia. En estas áreas, el riesgo de por vida de infección es más de un 60% siendo las infecciones en la niñez las más comunes. En las áreas de baja seropositividad (menos de un 2% de la población con anticuerpos anti-HBsAg), el riesgo de por vida de infección con VHB es menos de un 20% siendo las infecciones más frecuentes en adultos en grupos de riesgo alto. En los Estados Unidos, la seropositividad al HBsAg ocurre en menos de un 2% de la población pero en asiáticos americanos la VHB crónica puede estar en un 10-15% de la población. En asiáticos americanos, el carcinoma hepatocelular es la principal causa de muerte. La mitad de todos los niños nacidos de madres con infección crónica de VHB en América son asiáticos americanos. Los afro americanos también muestran un alta tasa de seropositividad para el VHB (figura 13).
El VHB se transmite por vías parenteral, sexual (hetero y homosexual) y neonatal. El virus está en grandes cantidades en sangre/suero y en heridas. Niveles moderados se encuentran en semen, saliva y secreciones vaginales. Otros fluidos corporales muestran unos niveles muy bajos o no-detectables.
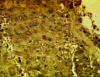 Figura 14 Inmunohistoquímica – positive para el antígeno de la Hepatitis B
Figura 14 Inmunohistoquímica – positive para el antígeno de la Hepatitis B
© Archivo de Imágenes Biomédicas de Bristol. Usado con autorización
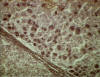 Figura 15
Figura 15
Cirrosis y antígeno de hepatitis B
© Archivo de Imágenes Biomédicas de Bristol. Usado con autorización
Diagnóstico
La hepatitis sérica es por lo general primero diagnosticada a partir de los síntomas clínicos. Las enzimas hepáticas también se detectan en el torrente sanguíneo durante la fase sintomática. Se puede obtener mayor información de la serología y de la presencia de antígenos del VHB. Por tanto, una infección aguda puede distinguirse de una crónica por la presencia de anticuerpos (IgM) contra el HBcAg. Los exámenes que detectan HBsAg y HBcAg y anticuerpos contra HBcAg, HBsAg y HBeAg (el panel de hepatitis B) se usan para el diagnóstico. Dada la gran cantidad de HBsAg que no se asocial a virus infectante, la presencia de HBeAg es el mejor marcados para virus infeccioso. También se muestra en la figura 10, que los anticuerpos anti-HBsAg no son detectables hasta más o menos ocho meses después de la infección mientras que el antígeno, HBsAg, es detectable mucho más temprano y luego remite. El fracaso en detectar anti-HBsAg en fases tempranas de la infección no es por la falta de anticuerpos; sino, que son indetectables porque se encuentran formando complejos con una gran cantidad de antígenos que es descamada de las células infectadas. El periodo que va desde los 6 a los 8 meses, en donde no pueden detectarse ni los HBsAg libres ni los anticuerpos se conoce como “la ventana HBsAg”. Este fenómeno también se aplica al HBeAg que es descamado de las células infectadas, aunque en mucho menor medida; entonces, la mejor herramienta para el diagnóstico de una infección aguda de VHB durante la ventana es la presencia de anti-HBc IgM. Para más información refiérase a la tabla 1.
El VHB también puede ser detectado en el laboratorio por inmunohistoquímica (figura 14-16).
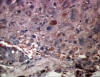 FFigura 16
FFigura 16Carcinoma hepatocelular y antígeno de la hepatitis B
© Archivo de Imágenes Biomédicas de Bristol. Usado con autorización
| Tabla 1 – En panel del VHB - Interpretación | ||
| Test | Resultados |
Interpretación |
| HBsAg anti-HBcAg anti-HBsAg |
Negativo Negativo Negativo |
El paciente es susceptible a una infección por VHB y aún no ha estado expuesto previamente al virus. El paciente no ha sido vacunado |
| HBsAg anti-HBcAg anti-HBsAg |
Negativo Positivo Positivo |
El paciente es inmune al VHB como resultado de haber sido infectado previamente (indicado por la presencia de anticuerpos anti-HBc lo cual no ocurre si el paciente es vacunado) |
| HBsAg anti-HBcAg anti-HBsAg |
Negativo Negativo Positivo |
El paciente es inmune porque fue vacunado contra el VHB |
| HBsAg anti-HBcAg anti-HBcAg IgM anti-HBsAg |
Positivo Positivo Positivo Negativo |
El paciente tiene una infección aguda de VHB. Cualquier anticuerpo anti-HBsAg que haya sido sintetizado ha formado complejos con la gran cantidad de antígenos descamados y por tanto es indetectable |
| HBsAg anti-HBcAg anti-HBcAg IgM anti-HBsAg |
Positivo Positivo Negativo Negativo |
El paciente tiene una infección crónica de VHB. La IgM anti-HBc ha disminuido |
| HBsAg anti-HBcAg anti-HBsAg |
Negativo Positivo Negativo |
El paciente puede encontrarse en una fase de recuperación de una
infección aguda de VHB. Este paciente puede estar infectado y por
tanto ser portador del VHB. La inhabilidad para detectar HBsAg puede
ser consecuencia de hallarse este en complejos con anticuerpos
anti-HBsAg en la fase de "ventana" |
 Figura 17
Figura 17Profilaxis postexposición recomendada para la exposición al VHB
CDC
Tratamiento
El mayor tratamiento son las medidas de mantenimiento. La inmunoglobulina anti-VHB es efectiva temprano luego de la exposición (figura 17). También puede administrarse neonatalmente a niños de madres HBsAg-positivas. Idealmente, la inmuno globulina debe de administrarse dentro de las 24 horas posterior al nacimiento o a la exposición y probablemente no es efectiva hasta una semana luego de la exposición.
Hay tres medicinas aprobadas por la FDA para el tratamiento de la Hepatitis B.
- Interferón-alfa 2b (Intron A - Schering-Plough) es un proteína que simula las defensas celulares naturales contra una infección viral.
- Hepsera (Adefovir Dipivoxil – Gilead Sciences) es un análogo de nucleótido que inhibe la ADM polimerasa del VHB (transcriptasa inversa). Su uso está indicado en el tratamiento de hepatitis B crónica en adultos con evidencia de replicación viral active y la evidencia de elevación persistente en las aminotransferasas séricas (ALT o AST) o enfermedad histológicamente activa.
- Lamivudina (Epivir HBV - Glaxo SmithKlein). Este es un 3TC el cual es un inhibidor de la transcriptasa inversa que también ha sido aprobado para el uso de infecciones con VIH. Al igual que con todos los inhibidores de la transcriptasa inversa, la aparición de mutantes resistentes es un problema. La Hepsera puede utilizarse en pacientes con virus mutantes resistentes a Epivir.
Vacunación
Esta es la mejor estrategia de prevención. Las vacunas actuales son subunidades sintetizadas en levadura que ha sido transfectada con un plásmido que contiene el gen S (que codifica para el HBsAg). La vacuna del VHB se vende bajo el nombre de Recombivax-HB (Merke) y Energix-B (Glaxo). Además, hay una vacuna aprobada contra tanto el VHA como el VHB (Twinrix – Glaxo). Otra formulación para niños (Pediarix – Glaxo) contiene vacunas contra difteria, tétanos, pertusis (tos ferina), polio y VHB.
Para vacunación de infantes, hay muchas opciones dependiendo de si la madre es HBsAg positivo. En este último caso, la vacuna se da junto con la inmunoglobulina del VHB. Si la madre es seronegativa, solo se administra la vacuna. Normalmente hay tres vacunas para niños (al nacimiento, y a los 1 y 6 meses) o adultos para proveer inmunidad protectora. La vacuna está recomendada para niños hasta los 18 años y para adultos en riesgo alto.
 Figura 18
Figura 18Agente de la Hepatitis Delta
CDC
HEPATITIS D – AGENTE DELTA
El virus de la Hepatitis D (VHD) o agente delta (figura 18) es un virus defectuoso con algunas similitudes con los viroides vegetales. No puede codificar su propia proteína de superficie y por ello, para producir más partículas víricas, necesita de un virus ayudante; este es el VHB. El VHD se adquiere junto con el VHB (co-infección) o como una sobre infección de un paciente ya infectado con el VHB.
La co-infección
por el VHD y el VHB exacerba la enfermedad aguda y es más posible la ocurrencia
de una hepatitis fulminante que si sólo se tratara del VHB. La posibilidad de
una infección crónica con el VHB es, no obstante, menor en personas co-infectadas.
La sobre-infección lleva a una más rápida manifestación de la enfermedad porque
la co-infección requiere de la replicación del VHB antes de que ocurra la
replicación del VHD. Los estudios del Centro de Control y Prevención de
Enfermedades (CDC, en inglés) muestran que los portadores del VHB
sobre-infectados con el VHD tienen un 70-80% de probabilidad de enfermedad
hepática crónica acompañada de cirrosis en comparación con el 15-30% en
pacientes sólo infectados con el VHB.
Transmisión
El VHD es usualmente transmitido por medios similares al VHB, esto es, el uso intravenoso de drogas y el contacto sexual, siendo este ultimo menos eficiente. La infección perinatal es infrecuente.
 Figura 19
Figura 19Curso serológico típico de una coinfección VHB - VHD CDC
 Figura 20
Figura 20
Sobre infección de VHD - VHB. Curso serológico típico CDC
Inmunología
En una co-infección VHB-VHD (figura 19), las IgG e IgM anti-VHD son generalmente vistas pero el antígeno del VHD solo se detecta en un cuarto de los pacientes. De verse el antígeno del VH desaparece cuando aparece el HBsAg. En una minoría de los pacientes, la IgM se encuentra temprano en una fase aguda o la IgG se observa más tarde. La elevación de los anticuerpos durante la fase sintomática declina a medida que se remiten los síntomas y, a diferencia de los anti-HBsAg, no hay anticuerpos que muestren que el paciente alguna vez estuvo infectado con el VHD. Al igual que como sucede con las infecciones simples con el VHB, los anti-HBsAg se eleven luego de que los niveles de antígeno han declinado con un periodo “ventana” entre ambos.
En una sobre-infección con el VHD (figura 20), los niveles de anti-HBsAg declinan a medida que se elevan los de anti-HDV. En este caso el antígeno del VHD y el virus (detectado por la presencia de su ARN) permanecen porque una sobre-infección generalmente implica una infección crónica de VHD. En esta infección crónica persisten los anticuerpos IgG e IgM contra el VHD.
Patología
Como sucede con las otras enfermedades de hepatitis viral, los síntomas son causados por la reacción inmunológica del paciente más que por los efectos citotóxicos directos de la infección viral en los hepatocitos. Hay una enfermedad más severa cuando el VHB sobre infecta un pacientes ya infectado por el VHB. En la sobre-infección de pacientes crónicamente infectados con el VHB, cerca de la mitad de los pacientes exhiben una hepatitis aguda que remite. Cerca del 10-40% tienen hepatitis persistente crónica y un 7-10% presentarán una hepatitis fulminante. En una co-infección, la mayoría de los pacientes (90%) manifiestan hepatitis aguda que remite y menos de un 10% tendrá una hepatitis crónica. Solo un 2-4% exhibe hepatitis fulminante. Por tanto, la hepatitis fulminante es más común en pacientes infectados con el VHD que en pacientes con otros virus de hepatitis.
 Figura 21
Figura 21Distribución geográfica de la Infección por el VHD CDC
Epidemiología
El VHD se encuentra a nivel mundial (figura 21) y puesto que la infección por VHB también es necesaria, la distribución es muy parecida a la del VHB. Cuando la incidencia de infección crónica de VHB es baja, la incidencia de VHD también lo es y primordialmente se ve en usuarios de drogas intravenosas. La tasa de infección por el VHD es variable en áreas con una tasa de VHB de moderada a alta. Por ejemplo, en Rusia, Rumania y en el sur de Italia, la infección por VHD es muy alta en pacientes infectados con el VHB. En otras partes de Italia y en el norte de África, el VHD es moderadamente común mientras que en el sur de Asia, con su altísima tasa de incidencia de VHB, la incidencia de VHD es baja. En algunos países sudamericanos hay epidemias periódicas aisladas de VHD en la población infectada por el VHB. Estos brotes pueden llevar a una enfermedad severa que implica una hepatitis fulminante con una tasa de fatalidad de 10-20%.
Diagnóstico
Hay análisis comerciales que detectan la IgG anti-VHD.
Tratamiento y Prevención
Dado que el VHD depende del VHB para producir una infección, la co-infección VHB/VHD puede ser prevenida por profilaxis para el VHB usando la muy efectiva vacuna contra el VHB. No hay profilaxis para la sobre-infección del VHD pero esta puede disminuirse con educación a pacientes infectados con el VHB tal como consejería contra el uso de drogas intravenosas.
 Figura
22
Figura
22
Incidencia estimada de Infección aguda de VHC, Estados Unidos, 1960-2001 CDC
 Figura
23
Figura
23
Prevalencia de la infección por VHC por edad y género, Estados Unidos,
1988-1994 CDC
HEPATITIS NO-A, NO-B (HNANB) - HEPATITIS C
El virus de la Hepatitis C (VHC) es un flavivirus para el cual los únicos reservorios conocidos son los humanos y los chimpancés; de hecho, el virus primero fue identificado en sangre de chimpancé. El VHC causa “hepatitis no-A, no-B” y era la principal causa de hepatitis post-transfusión antes de que los exámenes rutinarios en los bancos de sangre incluyeran los del VHC. A nivel mundial, hay aproximadamente 200 millones de portadores del VHC.
En los Estados Unidos, hay cerca de 2.4 a 3 millones de personas que están crónicamente infectadas con el VHC y entre 3.1 a 4.1 millones de personas han tenido una infección por VHC alguna vez en sus vidas. Hubo 25,000 infecciones nuevas del VHC en el 2001 (disminuyó de las 242,000 que hubo en 1985-89 como resultado de rastreos analíticos de sangre y la disminución de usuarios de drogas intravenosas) (figura 22); este virus causa el 40-60% de las enfermedades hepáticas crónicas implicando de 10,000 a 12,000 muertes por año. La seropositividad para el VHC es mayor en hombres en el grupo de edad de los 30-39 años (figura 23).
Aunque el VHC, al igual que el VHB, puede causar una hepatitis crónica persistente, las muertes por fallo hepático agudo son raras. La infección con el VHC usualmente es consecuencia de (figuras 24-26):
- Uso de drogas intravenosas. Esta es una ruta de infección bastante eficiente. Entre los drogadictos que comparten inyecciones y agujas, hay una prevalencia de un 30% de infección del VHC dentro de los 3 primeros años de iniciación en el hábito y de más de un 50% luego de los 5 años. La mayoría (del 50 al 90%) de los pacientes usuarios de drogas intravenosas infectados por el VIH también están infectados con el VHC.
- Transfusiones sanguíneas o transplantes de tejidos. Desde la introducción de las analíticas de rastreo viral, la incidencia de infecciones asociadas a transfusión han disminuido (figure 27).
- Exposición laboral a sangre y otros fluidos. Esto es algo ineficiente con una incidencia de infección de un 1.8% luego de un linchamiento con una aguja contaminada de un paciente VHC-positivo. Las salpicaduras de sangre o el contacto con alguna herida pueden resultar, aunque muy raro, en transmisión. El 1-2% de los profesionales de la Salud en los Estados Unidos son VHC-positivos (lo cual es menos que en la población general).
- Las transmisiones inadvertentes (iatrogénicas/nosocomiales) son resultado de inoculaciones
- Una madre infectada con el VHC al momento del parto. Cerca del 6% de los bebés nacidos de madres infectadas se infectan también y esto aumenta al 17% si la madre también está infectada con el VIH. No parece que el VHC pueda ser transmitido a través de la lactancia materna. Los niños infectados tienen un buen pronóstico y es muy rara una hepatitis C severa.
- Relaciones sexuales con una persona infectada. El riesgo aumenta con la promiscuidad pero la eficiencia del contagio es baja y lo que influencia su transmisión se desconoce. La transmisión de hombre a mujer es más eficiente que la de hombre a hombre; sin embargo, el VHC transmitido sexualmente constituye más o menos el 30% de las infecciones crónicas y agudas del VHC en los Estados Unidos.
 Figura 24
Figura 24Casos reportados de Hepatitis C aguda según factores de riesgo seleccionados, Estados Unidos, 1982-2001 CDC
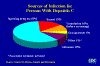 Figura 25 Fuentes de Infección para personas con Hepatitis
C CDC
Figura 25 Fuentes de Infección para personas con Hepatitis
C CDC
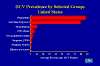 Figura 26 Prevalencia del VHC por grupos seleccionados Estados
Unidos CDC
Figura 26 Prevalencia del VHC por grupos seleccionados Estados
Unidos CDC
 Figura 27 Hepatitis C Post-transfusión CDC
Figura 27 Hepatitis C Post-transfusión CDC
PatogénesisEl VHC entra al torrente sanguíneo e infecta hepatocitos. El virus usualmente no mata la célula huésped y por tanto puede instaurar una infección persistente implicando una enfermedad crónica. Los síntomas, al igual que con el VHB, no son consecuencia del virus sino de los efectos del sistema inmune en los hepatocitos infectados, siendo la respuesta de las células T citotóxicas el factor más importante.
La viremia se detecta en una a tres semanas luego de la infección. Luego de una fase de pródromo de seis a siente semanas (aunque con un rango de dos a veintiséis semanas), los síntomas aparecen (ictericia, dolor abdominal, nausea, perdida del apetito, y oscurecimiento de la orina). Estos son usualmente mas leves que con el VHB y en más de 80% de los pacientes, la fase aguda de la viremia es asintomática. En la fase aguda de la infección, las partículas virales pueden ser detectadas por varios meses. En el 15-25% de los pacientes, el virus es depurado al final de la infección pero, en la mayoría de las personas infectadas, el VHC instaura una infección hepática persistente que puede durar por varios años implicando una hepatitis crónica activa. Muchos de estos pacientes desarrollan cirrosis hepática y algunos experimentan fallo hepático. Durante el periodo de infección crónica, el VHC puede dar paso a manifestaciones extra – hepáticas; estas incluyen crioglobulinemia mixta (resultando en eritema, vasculitis, etc.), porfiria cutánea retarda, glomérulo nefritis membranoproliferativa y posiblemente diabetes mellitus y linfoma. Estos síntomas puede deberse a complejos inmunes que se forman o a enfermedad autoinmune. La patogenicidad de las infecciones por el VHC se promueve bajo una variedad de condiciones incluyendo aumento en el consume de alcohol y co-infección con VIH o VHB crónica. Esta también es mayor en personas mayores (de más de 40 años) y del sexo masculino.
Carcinogénesis
Después de muchos años (casi treinta), una pequeña proporción (5%) de pacientes crónicamente infectados con VHC desarrollan carcinoma hepatocelular.
 Figura 28 Patrón serológico de una infección aguda del VHC y su recuperación
CDC
Figura 28 Patrón serológico de una infección aguda del VHC y su recuperación
CDC Figura 29 Patrón sexológico de una infección aguda de VHC que progresa a
infección crónica CDC
Figura 29 Patrón sexológico de una infección aguda de VHC que progresa a
infección crónica CDCInmunología
Cuando ocurren los síntomas, se extienden de uno a más de cinco meses luego de la infección; el virus es detectable en el torrente sanguíneo durante este periodo. También durante este periodo, las enzimas hepáticas, tales como la alanino aminotransferasa, se elevan (figura 28). Los anticuerpos anti-VHC aumentan luego de dos meses y son detectables por varios años si el pacientes está crónicamente infectado (figura 29) Hay seis serotipos del VHC que circulan a nivel mundial con múltiples subtipos.
Epidemiología
El VHC se encuentra a nivel mundial con la mayor incidencia en el sur y el centro de Europa, el Medio Oriente y Japón.
 Figura 30
Figura 30Algoritmo de exámenes de infección por VHC para el diagnóstico de personas asintomáticas CDC
Diagnóstico
Los síntomas son el primer aspecto del diagnóstico. Estos incluyen ictericia, nausea y fatiga acompañados de una elevación (de por los menos 10 veces) de la alanino aminotransferasa. Los anticuerpos contra el VHC también son claramente indicativos. Hay un test de ELISA altamente específico que detecta anticuerpos al VHC; no obstante, estos no aparecen hasta alas 8 a 20 semanas luego de la infección, lo cual es después del término de la fase de pródromo. Entonces, el anticuerpo no es un indicador confiable de infección aguda. Los métodos de PCR pueden ser usados para detectar el ARN viral en una semana o dos luego de la infección en pacientes seronegativos. También hay un estudio de inmunoblot recombinante que detecta dos o más anticuerpos del VHC. Se recomienda los exámenes analíticos para el VHC si el paciente ha usado drogas endovenosas, ha recibido factores de coagulación sintetizados antes de 1987, ha tenido algún transplante de órgano o transfusión sanguínea antes de 1992, ha sido sometido a hemodiálisis o muestra evidencia de enfermedad hepática. Las personas que han sido laboralmente expuestas a sangre infectada con el VHC o los niños de madres infectadas también debería de examinarse (figura 30).
La infección crónica puede ser diagnosticada por la presencia de anticuerpos y por elevación de larga data de las aminotransferasas séricas. Esto puede ser confirmado por PCR puesto que en una infección crónica, el ARN viral debe de estar presente en el torrente sanguíneo. En pacientes inmunosuprimidos, los exámenes de PCR son necesarios y este también es el caso cuando se sospechan comportamientos crónicos de perjuicio hepático, tales como alcoholismo. Otros problemas que pueden ser confundidos con hepatitis C son la hepatitis autoinmune, hepatitis B y D crónica, hepatitis alcohólica, esteatohepatitis no alcohólica (hígado graso), colangitis esclerosante, enfermedad de Wilson, enfermedad hepática relacionada con la deficiencia de alfa-1-antitripsina y enfermedad hepática inducida por drogas (Instituto Nacional de la Diabetes y los Problemas Digestivos y del Hígado, Instituto Nacional de la Salud).
Tratamiento
El paciente ha de se evaluado para enfermedad hepática crónica y aconsejado para que evite comportamientos tales como consume de alcohol, que puedan exacerbar el daño hepático. Dos drogas en combinación son recomendadas en un régimen de 24-48 semanas. Estas son ribavirina (refiérase a la sección de quimioterapia) e peginterferon alfa-2a y 2b (Peginterferon que tiene los nombres comerciales de Pegintron (Schering-Plough) y Pegasys (Roche)). Este último consiste en interferón humano recombinante unido a polietilenglicol lo que incrementa la vida media de la proteína en sangre permitiendo una inyección semanal (en vez de diaria) y mantiene unos niveles relativamente constantes de la droga. La ribavirina tiene poco efecto por sí sola sobre el VHC pero parece aumentar el efecto del interferón. Esta terapia de dos drogas causa la desaparición del ARN del VHC del torrente sanguíneo en casi el 70% de los pacientes y hay una disminución marcada en los niveles séricos de alaninoaminotransferasa; sin embargo, es necesario mantener el tratamiento puesto que muchos pacientes manifiestan recaída cuando detienen el uso de los medicamentos. Aquellos que exhiben una pérdida completa del ARN del VHC tanto durante el tratamiento como luego del mismo tienen menos probabilidad de recaída. La respuesta depende del genotipo del virus infectante. Desafortunadamente, este régimen farmacológico tiene mucho efectos colaterales.
Luego de la exposición la inmunoglobulina y interferón/ribavirina no se recomienda. En el caso de linchamientos con agudas etc., la fuente debe de evaluarse para VHC y el paciente ser referido a un especialista para su manejo.
HEPATITIS G
Al igual que el VHC, el VHG es un flavivirus. Poco se conoce del VHG pero puede causar hepatitis, aunque lo más probable es que no esté implicado en un número significativo de casos. En una encuesta realizada en Japón, tres de cada seis pacientes con hepatitis fulminante no-A, no-B, no-C, no-D, no-E fueron positivos serológicamente para la secuencia del ARN genómico del VHG. El VHG puede producir una infección aguda leve y la mayoría de los pacientes infectados progresan a una infección persistente, que probablemente no es clínicamente significativa. La transmisión es por contaminación sanguínea como por transfusión o drogas intravenosas. La hemodiálisis es un factor de riesgo. El diagnóstico es mediante anticuerpos o por la detección del ARN viral con PCR.
El virus GB (VGB, agente GB) fue aislado en los 1960's de un cirujano (identificado como GB) con hepatitis aguda (de la cual se recuperó) y fue demostrado la causa de hepatitis en monos tamarindos. Dos virus llamados VGB-A y VGB-B fueron aislados del suero de los monos tamarindos. Otros virus llamado VGB-C se encontró en un paciente en el Oeste de África. Los virus GB son flavivirus, igual que el VHG. Tienen un genoma de 9400 nucleótidos y la secuenciación muestra que el VGB-C tiene un 86% de similitud con el VHG a nivel de los nucleótidos y un 96% de similitud a nivel de los amino ácidos. El VHG y el VGB son por tanto diferentes aislados del mismo virus de hepatitis. Interesantemente, la co-infección de un paciente VIH positivo con el VGB parece proteger al paciente del VIH. Esto se da porque las infecciones con VGB resultan en un menor número de moléculas CCR5 en la superficie de los linfocitos T4 del paciente. El CCR5 es un co-receptor (junto al antígeno CD4) del VIH en las células T humanas. Desafortunadamente, parece ser que mientras que una co-infección de VIH y VGB-C protegen al paciente, cuando el paciente depura el VGB-C él/ella tiene mayor probabilidad de morir por la infección de VIH que algunas personas sin infección persistente del VGB-C. Más aún, la infección con el VGB reduce pero no elimina la expresión del CCR5 y también hay otros co-receptores que el VIH usa para entrar a la célula.
Regreso a la sección de Virologia Microbiología e Inmunología on line
Derechos de autor 2008 The Board of Trustees of the University of South Carolina
Esta página se modificó recientemente en Monday, March 10, 2008
Mantenimiento de la pagina por Richard Hunt
Favor de reportar problemas a rhunt@med.sc.edu